美國食品藥物管理局(FDA)在2025年3月14日宣布 Felycin-CA1 獲得條件性核准(Conditional Approval),可用於治療貓肥厚型心肌病變。這是全球首款專門針對貓肥厚型心肌病變的藥物,象徵獸醫心臟病治療的一大進展。
文章目錄
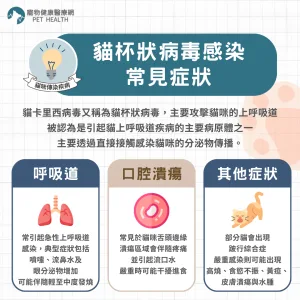
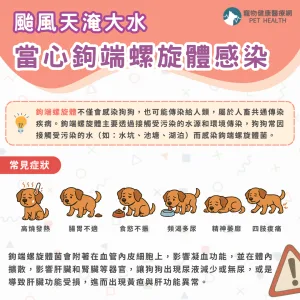
肥厚型心肌病變是貓咪常見致死性心臟病,臨床需求長期未被滿足
肥厚型心肌病變是貓最常見的心臟疾病,特別好發於緬因貓、拉格多貓、波斯貓等品種。此疾病會導致心臟左心室肌壁異常增厚,影響心臟功能,可能進一步發展為充血性心衰竭、動脈血栓、甚至猝死。
在過去,臨床上沒有專門針對肥厚型心肌病變的藥物,獸醫通常採用降血壓藥、β受體阻滯劑或利尿劑,但這些療法僅能緩解症狀,無法直接影響疾病進程。
(💡延伸閱讀:認識貓咪肥厚性心肌病變:常見症狀、治療方式及預後)
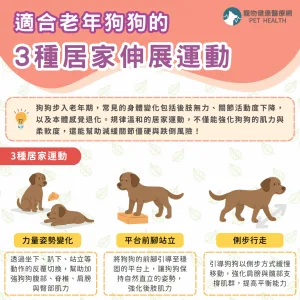
Felycin-CA1 的作用機制,如何抑制病程惡化

Felycin-CA1 由愛爾蘭 TriviumVet 公司所研發,主要成分為Sirolimus,是一種 mTOR(哺乳動物雷帕黴素標靶蛋白)抑制劑,可減緩心肌肥厚的進展。
- 劑量與使用方式:每週口服一次,劑量為 0.3 mg/kg。
- 安全性考量:此劑量不具免疫抑制作用,經 FDA 研究證實,不影響貓的疫苗免疫反應。
- 適用族群:僅限獸醫處方,使用前須篩檢肝功能,患有糖尿病或肝病的貓隻不可使用。
Felycin-CA1(Sirolimus)作用機轉
Sirolimus(又稱 Rapamycin)是一種 mTOR(哺乳動物雷帕黴素標靶蛋白) 抑制劑,透過調控 mTORC1 訊號通路來抑制異常的細胞生長與代謝活動。
▌mTORC1 活化與心肌病變
mTORC1 在心臟細胞內負責調控蛋白質與脂質合成,並影響細胞自噬。當受到慢性機械負荷(如:高血壓或基因突變)刺激時,mTORC1 過度活化,導致心肌細胞異常增殖與肥厚,進而引發心室壁增厚與心功能下降。
▌Sirolimus 抑制 mTORC1,延緩心肌肥厚
Sirolimus 能選擇性抑制 mTORC1 活性,降低蛋白質合成,恢復細胞自噬功能,並減少病理性心肌增厚。根據 RAPACAT 臨床試驗,每週口服低劑量 Sirolimus(0.3 mg/kg)可顯著降低貓左心室壁厚度,並減緩疾病進展,與安慰劑相比具有統計學上的顯著差異(p = 0.01)。
相關臨床研究
Felycin-CA1 的療效正在 HALT(Hypertrophic cardiomyopathy Advanced Long-term Treatment) 臨床試驗中進行驗證。該試驗為一項多中心、隨機、雙盲、安慰劑對照的臨床研究,目的在評估該藥物對貓隱性肥厚型心肌病(subclinical HCM) 的病程影響。
▌研究對象
- 經超音波診斷為 ACVIM Stage B1 或 B2 HCM 的貓隻
- 年齡介於 18 個月至 15 歲
- 體重 ≥2.5kg
- B2 期貓隻需接受Clopidogrel治療
▌研究設計
- 療程 12 個月,每週一次給藥
- 期間安排五次回診,檢查包括心臟超音波、心電圖、血壓測量與生物標記分析
該試驗預計能夠為獸醫心臟病領域提供首個針對貓肥厚型心肌病進程的實證數據,並進一步評估 Felycin-CA1 作為疾病治療藥物的潛力。(💡相關研究連結:https://www.hcmincats.com/halt)
FDA 為何批准為條件性核准?

根據 FDA 法規,條件性核准適用於治療嚴重或致命疾病,且難以進行大規模臨床試驗的藥物。Felycin-CA1 符合此標準,原因包括:
- 目前無現有專門療法,該藥填補市場空缺。
- 肥厚型心肌病變早期診斷困難,需透過超音波檢測,導致試驗收案不易。
- 疾病進展速度不一,部分貓存活數年,部分則迅速惡化,使試驗設計更具挑戰性。
Felycin-CA1 可先行上市,藥廠需在 5 年內提交完整療效數據,通過審查後才能獲得正式核准(Full Approval)。
Felycin-CA1 的推出,不僅對貓心臟病治療具有重大意義,也顯示動物用藥市場的發展潛力。隨著更多專業處方藥物進入市場,未來寵物醫療將更趨精細化與科學化。
參考資料
- FDA. (2025, March 14). FDA Conditionally Approves Drug for Management of Ventricular Hypertrophy in Cats. U.S. Food & Drug Administration. Retrieved from https://www.fda.gov/animal-veterinary/cvm-updates/fda-conditionally-approves-drug-management-ventricular-hypertrophy-cats
- Kaplan, J. L., Rivas, V. N., Walker, A. L., Grubb, L., Farrell, A., Fitzgerald, S., Kennedy, S., Jauregui, C. E., Crofton, A. E., McLaughlin, C., Van Zile, R., DeFrancesco, T. C., Meurs, K. M., & Stern, J. A. (2023). Delayed-release rapamycin halts progression of left ventricular hypertrophy in subclinical feline hypertrophic cardiomyopathy: results of the RAPACAT trial. Journal of the American Veterinary Medical Association, 261(11), 1628–1637. https://doi.org/10.2460/javma.23.04.0187

作者 – 寵物健康醫療網
寵物健康醫療網致力於打造台灣最健全的寵物專屬健康平台,提供最新的醫療指引、寵物健康知識與產業動態。